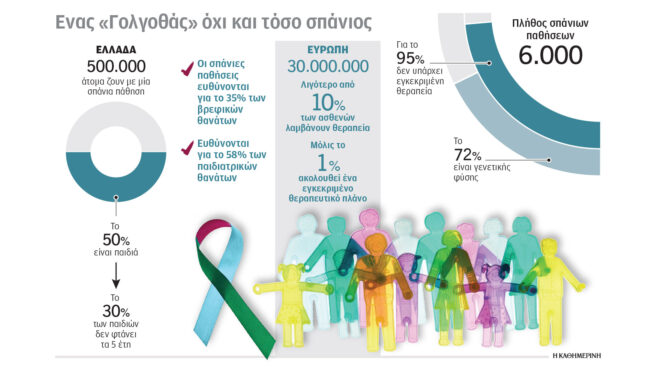
Ανήσυχοι έπειτα από τις αλλαγές που δρομολογεί το υπουργείο Υγείας σχετικά με την εισαγωγή στην Ελλάδα φαρμακευτικών σκευασμάτων που έχουν λάβει άδεια κυκλοφορίας μόνο στις ΗΠΑ ή σε άλλες χώρες της Ε.Ε. είναι περίπου 500.000 άνθρωποι που πάσχουν από σπάνια νοσήματα. Η συζήτηση για τη θέσπιση ενός πιο αυστηρού πλαισίου αδειοδότησης ξεκίνησε με αφορμή το φάρμακο Relyvrio, το οποίο κατά την κλινική μελέτη της τρίτης φάσης κρίθηκε αναποτελεσματικό και πρόκειται να αποσυρθεί από την αγορά. «Η θεραπεία αφορούσε όσους ανθρώπους πάσχουν από ALS (πλάγια μυατροφική σκλήρυνση), οι οποίοι έχουν προσδόκιμο ζωής δύο χρόνων και για τους οποίους δεν διατίθεται καμία άλλη θεραπεία», λέει στην «Κ» ο πρόεδρος της Ενωσης Σπανίων Ασθενών Ελλάδος, κ. Δημήτρης Αθανασίου, εξηγώντας το σκεπτικό με το οποίο λειτουργεί το σύστημα «πρώιμης πρόσβασης» σε νέα θεραπευτικά πρωτόκολλα. «Πρόκειται για κρίσιμο εργαλείο, που πρέπει να διατηρηθεί χωρίς προσκόμματα. Ζυγίζεται πάντοτε η πιθανή ωφέλεια με το πιθανό ρίσκο, που μπορεί να συνεπάγεται η χορήγηση ενός φαρμάκου σε ανθρώπους με θανατηφόρες ασθένειες και περιορισμένο προσδόκιμο ζωής», τονίζει ο ίδιος.
Η «άδεια επείγουσας πρόωρης χρήσης» μπορεί στην περίπτωση του Relyvrio να μην έφερε τα επιθυμητά αποτελέσματα και επιπλέον να συνδέεται με την καταβολή πολύ υψηλών ποσών, σε άλλες ωστόσο περιπτώσεις η ενεργοποίηση αυτού του μηχανισμού έσωσε ζωές. «Χαρακτηριστικό παράδειγμα είναι ο μικρός Ραφαήλ», λέει ο κ. Αθανασίου, «για τον οποίο το 2019 δεν δόθηκε άδεια επείγουσας πρόωρης χρήσης, αλλά συγκεντρώθηκε το απαιτούμενο ποσό μέσω fundraising για να μεταβεί στις ΗΠΑ. Εκεί το παιδί εντάχθηκε σε θεραπευτικό πρόγραμμα και σήμερα είναι μεταξύ μας». Πολλά άλλα παιδιά –κάθε χρόνο γεννιούνται στην Ελλάδα 8-9 παιδιά με την εν λόγω ασθένεια– δεν κατάφεραν να επιζήσουν, «καθώς το προσδόκιμο είναι 16 μήνες». «Ευτυχώς, τα επόμενα χρόνια ελήφθη η σχετική απόφαση, το φάρμακο εισήχθη στην Ελλάδα, και χορηγήθηκε στα βρέφη με νωτιαία μυϊκή ατροφία, τα οποία σώθηκαν», υπογραμμίζει ο κ. Αθανασίου.
Αντίστοιχη «ιστορία επιτυχίας» αποτελεί και η ένταξη ασθενών με κυστική ίνωση σε πρόγραμμα με «άδεια πρώιμης πρόσβασης». «Ας μην ξεχνάμε ότι και τα εμβόλια για τον κορωνοϊό μπόρεσαν να κυκλοφορήσουν χάρη σε αυτόν τον μηχανισμό». Ο Ευρωπαϊκός Οργανισμός Φαρμάκων (EMA) και ο Οργανισμός Τροφίμων και Φαρμάκων (FDA) έχουν αναπτύξει ειδικά προγράμματα που στοχεύουν στην επιτάχυνση των διαδικασιών αξιολόγησης και έγκρισης νέων φαρμάκων· συχνά, τα νέα φάρμακα για ακάλυπτη ιατρική ανάγκη λαμβάνουν πρώτα την έγκριση στις ΗΠΑ, με τον FDA να διενεργεί τις αναγκαίες αξιολογήσεις ταχύτερα από τον EMA. «Ο FDA, ως μια καταξιωμένη ρυθμιστική αρχή, λειτουργεί ως καταλύτης στη διαδικασία τής “υπό όρους έγκρισης” φαρμάκων στις υπόλοιπες χώρες», επισημαίνει ο κ. Αθανασίου, που έχει διατελέσει για έξι χρόνια μέλος της παιδιατρικής επιτροπής του Ευρωπαϊκού Οργανισμού Φαρμάκων. «Τα νέα φάρμακα στηρίζονται σε πολύ προηγμένες τεχνολογίες, που απαιτούν εξειδικευμένη τεχνογνωσία», εξηγεί, «ο EMA και ο FDA διαθέτουν ειδικές επιστημονικές επιτροπές για αυτό· εκτιμώ ότι αυτή η διαδικασία είναι δύσκολο να γίνει σε εθνικό επίπεδο, όπως προβλέπει η νέα τροπολογία».
Η «πρώιμη» πρόσβαση σε νέα θεραπευτικά πρωτόκολλα είναι μονόδρομος για ανθρώπους με περιορισμένο προσδόκιμο ζωής, εξηγεί ο πρόεδρος της Ενωσης Σπανίων Ασθενών Ελλάδος.
Χωρίς θεραπεία το 95%
Δυστυχώς, οι ασθενείς με σπάνιες ασθένειες που έχουν την ευκαιρία μιας θεραπείας είναι η μειονότητα, καθώς για το 95% των ασθενειών δεν διατίθεται κανένα θεραπευτικό σχήμα. «Πολύ λίγοι παίρνουν μόνον φάρμακα που θεραπεύουν, καθυστερούν την εξέλιξη της νόσου ή βελτιώνουν την ποιότητα ζωής», σημειώνει ο κ. Αθανασίου, που έχει παιδί με μυϊκή δυστροφία duchenne. Συχνά, αυτά τα σκευάσματα είναι δυσεύρετα. «Δεν πρόκειται για έλλειψη, αλλά για απουσία σχεδιασμού», απαντά ο πρόεδρος της Ενωσης. «Ο αριθμός των πασχόντων είναι συγκεκριμένος και αντίστοιχα οι ανάγκες τους, το υπουργείο έχει τη δυνατότητα να παραγγέλνει εγκαίρως συγκεκριμένες ποσότητες και να κάνει σχετικές διαπραγματεύσεις για την τιμή των φαρμάκων». Ακριβώς επειδή οι ασθενείς του κάθε σπάνιου νοσήματος είναι μετρημένοι στα δάκτυλα και έχουν γενετικές διαγνώσεις, «δεν είναι ρεαλιστικό το ενδεχόμενο της υπερσυνταγογράφησης, για το οποίο έγινε λόγος τις προηγούμενες μέρες», τονίζει ο κ. Αθανασίου. Στο πλαίσιο αυτό, άλλωστε, η Ενωση έχει πολλάκις προτείνει τη θέσπιση ενός Μητρώου Σπανίων Ασθενών αλλά και την εφαρμογή ενός εθνικού σχεδίου δράσης για τα σπάνια νοσήματα. Τέλος, εκφράζεται το αίτημα να συμμετάσχει η Ενωση στις προγραμματισμένες συναντήσεις στο υπουργείο Υγείας μαζί με όλους τους εμπλεκόμενους φορείς, όπως γίνεται στις επιτροπές του ΕΜΑ.
Στελέχη του υπουργείου Υγείας σχολιάζοντας τις ανησυχίες της Ενωσης Σπανίων Ασθενών Ελλάδος, ανέφεραν στην «Κ» ότι με τροπολογία που ψηφίστηκε την προηγούμενη εβδομάδα «συστήνεται μια επιτροπή ελέγχου του Συστήματος Ηλεκτρονικής Προέγκρισης για τον περιορισμό της φαρμακευτικής δαπάνης και υπερσυνταγογράφησης· το έργο της θα είναι ο προέλεγχος όλων των αιτημάτων εισαγωγής ακριβών φαρμακευτικών σκευασμάτων που παραγγέλνονται και παραλαμβάνονται από το εξωτερικό μέσω του Ινστιτούτου Φαρμακευτικής Ερευνας και Τεχνολογίας (ΙΦΕΤ), τα οποία αποζημιώνονται εξ ολοκλήρου από τον ΕΟΠΥΥ. Η κατάθεση της τροπολογίας για τη σύσταση της επιτροπής κρίθηκε επιβεβλημένη μετά τη διαπίστωση ότι ξοδεύτηκαν στην Ελλάδα 15 εκατ. ευρώ για την εισαγωγή στη χώρα πανάκριβης θεραπείας που αποδείχθηκε αναποτελεσματική και αποσύρθηκε».